Sociedade do Lítio:
da água do mar ao hidrogênio
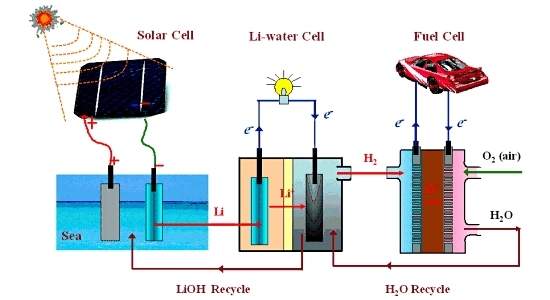
Cientistas japoneses descobriram uma forma de armazenar quimicamente a luz do Sol e depois utilizá-la para quebrar as moléculas de água e produzir hidrogênio de uma forma limpa e sustentável. [Imagem: ChemSusChem]
Cientistas japoneses descobriram uma forma de armazenar quimicamente a luz do Sol e depois utilizá-la para quebrar as moléculas de água e produzir hidrogênio de uma forma limpa e sustentável.
Embora estejam sendo feitos progressos nas células a combustível, uma espécie de gerador capaz de produzir eletricidade a partir do hidrogênio ou etanol, gerando apenas água como subproduto, a produção do hidrogênio ainda é um gargalo a ser vencido caso se queira que o gás torne-se algum dia o combustível do presente.
Até lá, o hidrogênio permanecerá como um combustível do futuro.
Rota química
Agora, a equipe do professor Haoshen Zhou, do Instituto de Pesquisas em Tecnologias Energéticas, do Japão, descobriu como usar uma rota química para produzir hidrogênio.
E, o que parece ser ainda mais vantajoso, o novo processo não gera apenas o gás, mas também produz eletricidade.
Os cientistas usaram o mesmo processo que já espantou milhões de estudantes ao redor do mundo, no qual o professor de química demonstra a violenta reação entre o sódio e a água, na qual o sódio é reduzido.
Hidrogênio e eletricidade
Os metais que demonstram esse comportamento são os chamados metais alcalinos, um grupo que inclui também o potássio, o césio, e o lítio - o mesmo lítio das baterias recarregáveis.
O que a equipe do Dr. Zhou fez foi controlar a reação entre o lítio e a água, mantendo-a no interior de um sistema fechado.
No processo controlado, dois objetivos podem ser atingidos simultaneamente: a reação química gera hidrogênio e ainda produz uma corrente elétrica que pode ser aproveitada.
Célula de combustível
O processo funciona em uma espécie de célula de combustível fechada, composta por dois compartimentos separados por uma membrana: um compartimento contém uma solução de lítio (anodo) em um solvente orgânico, enquanto o outro contém uma solução aquosa com um eletrólito (catodo).
A oxidação do lítio gera elétrons, que fluem do anodo para o catodo, produzindo uma corrente elétrica.
Quando os elétrons chegam ao catodo, eles reduzem a água, quebrando a molécula para produzir oxigênio e hidrogênio. O controle da corrente elétrica que flui ao longo da célula também controla a taxa de geração do hidrogênio.
Armazenando a luz do Sol
Outro aspecto atrativo desta tecnologia é que o lítio metálico pode ser produzido a partir de soluções salinas (por exemplo, água do mar), usando a luz solar.
Em outras palavras, a energia do Sol pode ser "armazenada" no metal, e usada quando necessário na reação do lítio no interior da célula de combustível.
Recarregar essa "bateria" seria uma questão de substituir a célula de lítio metálico - para comparação, veja outra tecnologia que permite "completar a bateria" na reportagem Baterias poderão ser reabastecidas com carga.
Sociedade do lítio
"O lítio, que já é largamente utilizado nas baterias de íons de lítio, e também será usado no futuro nas células de combustível de ar-lítio e neste novo sistema de célula lítio-água/hidrogênio/combustível, poderá levar a humanidade a uma 'sociedade do lítio' totalmente sustentável, baseada em redes inteligentes de produção de energia a partir do lítio," vislumbra o Dr. Zhou.
Vários grupos de pesquisadores ao redor do mundo trabalham na utilização da luz do Sol para produzir eletricidade limpa e hidrogênio. A maioria dos esforços até agora se concentrava nos processos conhecidos como fotossíntese artificial.
Esta é a primeira vez que se demonstra que o lítio pode ser a base para a produção totalmente sustentável de energia.
A teoria prevê que o hidrogênio metálico será um supercondutor de alta temperatura. Um supercondutor é um estado da matéria onde os elétrons - e, portanto, a eletricidade - pode fluir indefinidamente e sem resistência. Os supercondutores conhecidos somente funcionam em temperaturas criogênicas.
Agora, um novo estudo teórico prevê que a metalização de misturas gasosas ricas em hidrogênio poderá ocorrer sob pressões significativamente mais baixas.
O hidrogênio e o lítio - usado em baterias recarregáveis - são o primeiro e o terceiro elementos mais leves no universo, respectivamente. Sob a pressão e a temperatura normais encontradas na Terra, o hidrogênio é um gás e o lítio é um metal.
No gás hidrogênio, os átomos são fortemente ligados em pares, com cada átomo de hidrogênio contribuindo com um elétron para a ligação. É por isso que, no mundo da química, o hidrogênio é conhecido por H2 - uma molécula formada pela forte ligação dos dois átomos de hidrogênio.
O hidrogênio e o lítio normalmente reagem entre si, formando um composto estável. Este composto de lítio-hidrogênio, ou LiH, não é metálico.
Os pesquisadores vêm tentando arrancar um elétron do hidrogênio comprimindo-o sob as faces de uma célula de pressão - conhecida como bigorna de diamante - já tendo alcançado pressões de 3,4 milhões de atmosferas. A pressão ao nível do mar na Terra equivale a uma atmosfera. A pressão no centro da Terra tem cerca de 3,5 milhões de atmosferas. Os cientistas não tiveram sucesso em alcançar essa pressão com esse método de pressão constante. Mas eles conseguiram com técnicas de ondas de choque. E nem assim alcançaram o tão sonhado hidrogênio metálico.
Os simuladores computacionais calcularam que o hidrogênio poderá se metalizar pela combinação de um átomo de lítio com vários átomos de hidrogênio, sob as pressões alcançáveis em laboratório.
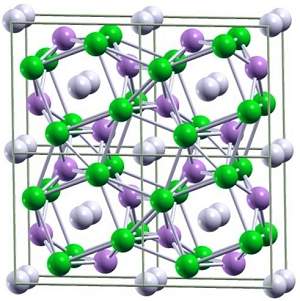
Uma das combinações estudadas contém um átomo de lítio para cada seis átomos de hidrogênio, formando o LiH6, um composto que não ocorre naturalmente na Terra.
Os cálculos preveem que, nesse composto hipotético, o átomo de lítio libera o elétron de sua camada mais externa, que é alocado entre as três moléculas de H2.
Sob pressão, a reação forma um composto de hidrogênio metálico estável.
"O composto metálico LiH6 deverá se tornar estável sob uma pressão de cerca de 1 milhão de atmosferas, o que é cerca de 25 por cento da pressão exigida para metalizar o hidrogênio sozinho," explica Eva Zurek, principal autora do artigo.
"O que é muito interessante é que, entre 1 e 1,6 milhão de atmosferas, todas as combinações de lítio e hidrogênio são estáveis ou metaestáveis e todas são metálicas," disse Roald Hoffmann, coautor do estudo.
Se tiverem sucesso, o estudo representará um passo importante ao demonstrar a possibilidade de combinações não-tradicionais de elementos leves, levando não apenas à fabricação do longamente sonhado hidrogênio metálico, como também à descoberta de novos materiais e novos estados da matéria.
Uma pitada de lítio cria hidrogênio metálico supercondutor
National Science Foundation - 16/10/2009

Modelo previsto do cristal de lítio-hidrogênio. Átomos de lítio estão em verde, pares de hidrogênio estão em branco e os íons negativos de hidrogênio estão em roxo.[Imagem: Eva Zurek]
Hidrogênio metálico
A ciência tem uma longa história de insucessos nas tentativas de criar hidrogênio sólido, transformando o gás em um metal pela aplicação de pressões incrivelmente elevadas.A teoria prevê que o hidrogênio metálico será um supercondutor de alta temperatura. Um supercondutor é um estado da matéria onde os elétrons - e, portanto, a eletricidade - pode fluir indefinidamente e sem resistência. Os supercondutores conhecidos somente funcionam em temperaturas criogênicas.
Agora, um novo estudo teórico prevê que a metalização de misturas gasosas ricas em hidrogênio poderá ocorrer sob pressões significativamente mais baixas.
Uma pitada de lítio
Adicionando pequenas quantidades de lítio ao hidrogênio, os cientistas calculam que o sistema resultante poderá ser metalizado sob uma pressão equivalente a um quarto da pressão prevista para a solidificação do hidrogênio puro.O hidrogênio e o lítio - usado em baterias recarregáveis - são o primeiro e o terceiro elementos mais leves no universo, respectivamente. Sob a pressão e a temperatura normais encontradas na Terra, o hidrogênio é um gás e o lítio é um metal.
No gás hidrogênio, os átomos são fortemente ligados em pares, com cada átomo de hidrogênio contribuindo com um elétron para a ligação. É por isso que, no mundo da química, o hidrogênio é conhecido por H2 - uma molécula formada pela forte ligação dos dois átomos de hidrogênio.
O hidrogênio e o lítio normalmente reagem entre si, formando um composto estável. Este composto de lítio-hidrogênio, ou LiH, não é metálico.
Pressão planetária
Acredita-se que o hidrogênio metálico esteja presente no interior de planetas como Júpiter e Saturno, por causa das intensas forças gravitacionais e das pressões encontradas em seus núcleos.Os pesquisadores vêm tentando arrancar um elétron do hidrogênio comprimindo-o sob as faces de uma célula de pressão - conhecida como bigorna de diamante - já tendo alcançado pressões de 3,4 milhões de atmosferas. A pressão ao nível do mar na Terra equivale a uma atmosfera. A pressão no centro da Terra tem cerca de 3,5 milhões de atmosferas. Os cientistas não tiveram sucesso em alcançar essa pressão com esse método de pressão constante. Mas eles conseguiram com técnicas de ondas de choque. E nem assim alcançaram o tão sonhado hidrogênio metálico.
Reações simuladas
Como o hidrogênio insiste em não se metalizar sob as condições atualmente alcançáveis em condições de laboratório, os pesquisadores passaram a usar sofisticados programas de computador para simular as condições alcançáveis e o que ocorre em cada uma delas.Os simuladores computacionais calcularam que o hidrogênio poderá se metalizar pela combinação de um átomo de lítio com vários átomos de hidrogênio, sob as pressões alcançáveis em laboratório.
Uma das combinações estudadas contém um átomo de lítio para cada seis átomos de hidrogênio, formando o LiH6, um composto que não ocorre naturalmente na Terra.
Os cálculos preveem que, nesse composto hipotético, o átomo de lítio libera o elétron de sua camada mais externa, que é alocado entre as três moléculas de H2.
Sob pressão, a reação forma um composto de hidrogênio metálico estável.
Múltiplas opções
Os cientistas também calculam que o LiH6 pode se tornar um metal sob pressões normais. Entretanto, sob essas condições, ele não é estável e se decompõe para formar LiH e H2."O composto metálico LiH6 deverá se tornar estável sob uma pressão de cerca de 1 milhão de atmosferas, o que é cerca de 25 por cento da pressão exigida para metalizar o hidrogênio sozinho," explica Eva Zurek, principal autora do artigo.
"O que é muito interessante é que, entre 1 e 1,6 milhão de atmosferas, todas as combinações de lítio e hidrogênio são estáveis ou metaestáveis e todas são metálicas," disse Roald Hoffmann, coautor do estudo.
Novos estados da matéria
Os cientistas responsáveis pela simulação teórica já estão em contato com seus colegas experimentalistas, discutindo a melhor abordagem para fabricar o composto. Segundo estes, a melhor abordagem será começar com o composto LiH, adicionando-se átomos de hidrogênio, um de cada vez.Se tiverem sucesso, o estudo representará um passo importante ao demonstrar a possibilidade de combinações não-tradicionais de elementos leves, levando não apenas à fabricação do longamente sonhado hidrogênio metálico, como também à descoberta de novos materiais e novos estados da matéria.
Fonte:
Redação do Site Inovação Tecnológica
- 01/06/2010
INOVAÇÃO Tecnológica - ENERGIA
http://www.inovacaotecnologica.com.br/noticias/noticia.php?artigo=sociedade-do-litio-agua-mar-hidrogenio&id=010115100601&ebol=sim


Nenhum comentário:
Postar um comentário
Quer comentar,o espaço é todo seu!